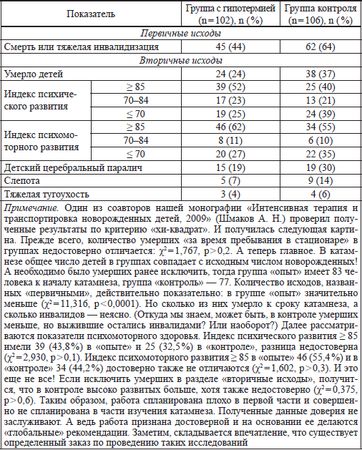
В возрасте 18–22 месяцев жизни дети были обследованы в катамнезе. Результаты катамнестического исследования приведены в таблице 2. Как видно из таблицы, в целом дети, перенесшие тяжелую гипоксию, но в комплексе лечебных мероприятий получавшие церебральную гипотермию, имели лучшие исходы, чем дети, не перенесшие "лечебную" гипотермию. А теперь обещанные комментарии… (см. примечание к таблице 2).
Несмотря на данную работу и множество других, посвященных лечению гипотермией последствий тяжелой асфиксии, даже авторы значительных рандомизированных исследований, например Edwards A. D., Azzopardi D. V. (2006), продемонстрировавшие снижение летальности и тяжелой инвалидизации после перенесенного тяжелого постгипоксического синдрома, считают, что в настоящее время нет достаточного количества наблюдений и исследований, позволяющих рекомендовать данный метод для рутинного клинического использования. Более того, начинают накапливаться сведения о побочных эффектах церебральной гипотермии.
Так, Navarini-Meury S. et al. (2007) сообщают о таком "новом" побочном эффекте у охлажденных детей, как склерема. В 2003 году в ряде работ (Henderson W. R. et al., 2003; McIntyre L. A. et al., 2003; Alderson P. et al., 2003) продемонстрировано увеличение частоты септических осложнений у охлажденных больных. Связаны указанные осложнения с нарушением функции нейтрофилов, в частности, ухудшением их миграции, что было доказано в экспериментальных работах уже достаточно давно (Biggar W. et al., 1986). Кроме того, по крайней мере у взрослых больных, гипотермия приводит к выраженной гиперпродукции провоспалительных цитокинов: ФНО и ИЛ-6 (Arons М. М. et al., 1999). В 2005 году Mathur N. В. et al. показали, что летальность детей после перенесенной тяжелой гипотермии составляет 80 %, а после незначительной гипотермии – 39,3 %. Если же умеренная гипотермия сочеталась с гипогликемией (авторы рассматривают вторую как осложнение первой), то летальность в группе таких детей увеличивалась практически в 2 раза и составляла 71,4 %.
Как отмечает Д. Н. Сурков (2012), при трактовке этого осложнения очень важным вопросом является: какая проводилась инфузионная терапия? Рестриктивная или либеральная? Достаточно давно известно (В. В. Подвысоцкий, 1905), что при проведении гипотермии снижается скорость обменных процессов. Логично предположить, что у таких детей не могут применяться обычные расчеты физиологической потребности в жидкости (хотя этот вопрос практически не исследован в неонатальной практике). А если их постоянно "переливать", а это может происходить "незаметно", то это, естественно, будет приводить к секвестрации избыточной жидкости, поскольку клубочковая фильтрация и диурез (количество мочи) у таких детей всегда снижены. Второй вопрос, что в условиях сниженной (не нарушенной, а именно сниженной) периферической перфузии нельзя ни охлаждать, ни согревать детей контактным методом. В первом случае возникнет "холодный" некроз (обморожение), во втором – контактный ожог (даже если поверхность не будет очень горячей, достаточно градиента температур кожи и нагретой поверхности более 10 градусов). Так что, наверное, пассивная гипотермия (обдув, конвекция) безопаснее активной кондукционной (на матрасиках). Вероятно, еще лучший способ – внутривенное охлаждение, как при АИК.
В 2010–2011 годы появились сообщения (Oza V. et al., 2010; Hogeling М. et al., 2011) об обширных некрозах подкожно-жировой клетчатки (спины, головы, рук) у детей с гипоксически-ишемической энцефалопатией, лечившихся методом терапевтической гипотермии.
Christensen R. D. et al. (2011) описали нарушения функций тромбоцитов у 60 % детей, пролеченных с помощью "активной" гипотермии, проявившиеся геморрагическим синдромом различной локализации. Геморрагический синдром возник в первые 24 часа жизни младенцев. Функции тромбоцитов восстановились после согревания ребенка. Израильские коллеги (Landau Y. et al., 2011) кровоточивости не описывают, но, применив гипотермию у 6 детей с постгипоксической энцефалопатией в первые часы жизни (средний возраст 4,2 часа от рождения), они отметили гиперкальцемию у одного ребенка, некрозы подкожно-жировой клетчатки – у одного новорожденного, пневмоторакс – у одного, синдром аспирации – у двух младенцев. В заключение работы, правда, они пишут, что в среднем возрасте 7,2 месяца жизни дети показывают удовлетворительное неврологическое развитие и отсутствие судорожного синдрома. Но, заметим, что вряд ли можно оценивать катамнез через такой короткий срок.
Наконец, в 2011 году, подводя некоторые итоги применения церебральной гипотермии в течение десятилетия, специалисты одной из ведущих неонатальных клиник в США Bonifacio S. L. et al. в большой обзорной работе указывают: "Терапия, направленная на снижение неврологических осложнений у детей, перенесших асфиксию, сделала гипотермию стандартным лечением. Однако эта терапия не обеспечивает полной защиты при возникновении неврологических осложнений и диктует необходимость разработки вспомогательной терапии для улучшения неврологического результата". Им вторят Johnston М. V. et al. (2011) из Балтимора, Leone Т. A., Finer N. N. (2011) из Сан-Диего и т. д.
Добавим от себя, что необходимы клинические, лабораторные или функциональные методы исследования, позволяющие оценить эффективность гипотермии и прогноз тяжести постгипоксической энцефалопатии. Какие же показатели и методы предлагаются для оценки тяжести состояния и эффективности гипотермии? Единодушного мнения на этот счет нет. Предлагаются ЭЭГ (Wusthoff С. J. et al., 2011), индекс резистентности сосудов головного мозга (Elstad М. et al., 2011), чередование циклов сон-бодрствование (Takenouchi Т. et al., 2011), видео-мониторинг ЭЭГ (Nash К. В. et al., 2011), концентрация глюкозы крови (Nadeem М. et al., 2011), эхокардиография (Kluckow М., 2011), уровень нейрон-специфической энолазы (Yamada К. et al., 2011) и т. д. Пока, к сожалению, эффективность этих методов оценки эффективности церебральной гипотермии у детей не является общепризнанной, поскольку, зачастую не позволяет строить долгосрочный прогноз. Например, показатели ЭЭГ коррелируют со смертельным исходом, но не всегда ассоциированы с неблагоприятным исходом постгипоксической энцефалопатии (Hamelin S. et al., 2011) и т. д.
Отсутствие эффективности данного метода у части детей также пытаются объяснить по-разному. Заметим от себя, что, по нашему убеждению, ни один из терапевтических методов, применяемых в медицине, в том числе и неонатологии, не может обладать 100 %-й эффективностью. Но где тот предел эффективности, который позволяет рекомендовать применение того или иного метода в клиническую практику? Хорошо бы ответить на этот вопрос. Вероятно, для разных методов этот предел неодинаковый. Тем не менее, изучение церебральной гипотермии значительно расширяет наши представления о многих патологических процессах у новорожденных детей. Так, в некоторых работах неэффективность церебральной гипотермии пытаются объяснить внутриутробным поражением плода, в частности инфекционного генеза, который можно диагностировать по поражению плаценты (Wintermark P. et al., 2011).
На наш взгляд, данные результаты перекликаются с достаточно давно проведенными исследованиями в нашей стране и за рубежом. И отражают общие закономерности, в том числе встречающиеся и в неонатальной медицине. Например, выяснение механизмов поражения ЦНС при неонатальных гипербилирубинемиях выявило ряд закономерностей. Напомним читателю факт хорошо известный из клинической практики. Хоть возникновение "ядерной желтухи" у новорожденных и зависит от уровня непрямого билирубина (НБ) в плазме крови, но не всегда у детей с одинаковой массой тела, сроком гестации и даже одинаково высоким уровнем билирубина возникает поражение мозга. Большое значение в развитии билирубиновой энцефалопатии имеют факторы риска. Например, факторы, увеличивающие проницаемость гематоэнцефалического барьера, такие как гиперосмолярность, метаболический ацидоз, артериальная гипертензия и т. д. По нашему мнению, должны быть выделены такие же "факторы риска" или "факторы неэффективности" различных методов, применяемых для лечения новорожденных детей. Это может быть одной из приоритетных научных задач неонатологии.
Исследования по применению гипотермии у новорожденных имеют большое значение и для неонатальной фармакологии. Имеются попытки использования различных лекарственных препаратов, усиливающих действие терапевтической гипотермии. Filippi L. et al. (2011) обследовали 19 новорожденных, перенесших тяжелую асфиксию, имевших в структуре постгипоксической энцефалопатии судорожный синдром. Применялась церебральная гипотермия. Им также был назначен фенобарбитал в возрастных дозировках для купирования судорожного синдрома. Оценка фармакодинамики фенобарбитала при охлаждении позволила авторам работы сделать вывод, что пиковые концентрации препарата в крови значительно более высокие, чем у детей с судорожным синдромом, не получавших терапевтическую гипотермию. У охлажденных детей также увеличивался период полураспада препарата, составляя 173,9 ±62,5 часа. На наш взгляд, это необходимо учитывать при проведении терапии охлаждением. Вполне возможно и другие препараты меняют фармакодинамику при охлаждении, что, по нашему мнению, требует дальнейших и более широких исследований.
Конечно, не только фенобарбитал применяется для лечения постгипоксической энцефалопатии. Имеются попытки применения с целью нейропротекции блокаторов ионных каналов (ксенон), антиоксидантов (аллопуринол, индометацин), антивоспалительных цитокинов (эритропоэтин, мелатонин), блокаторов апоптоза (ядерный фактор каппа) и т. д. (Fan X., van Bel F., 2010).