2.1. Общие вопросы теплорегуляции
Теплорегуляция – это поддержание баланса между потерями тепла и теплопродукцией. К концу XIX столетия стало ясно (Landois L., Rosemann R., 1900), что высвобождающаяся при биологическом окислении (сгорании) энергия питательных веществ (или при голодании материал, отдаваемый самим организмом) превращается в тепло. В настоящее время понятно, что тепло – "побочный продукт" метаболических процессов, и хотя скорость биологического окисления возрастает при увеличении температуры и, следовательно, увеличивается теплообразование, но в норме температура тела остается стабильной. Это вызвано тем, что прирост температуры тела приводит к увеличению отдачи тепла организмом. То есть, как и при рассмотрении любого физиологического процесса, мы видим удивительное сохранение баланса, в данном случае баланса между теплопродукцией и теплоотдачей, позволяющего организму сохранять относительно постоянную температуру тела.
Суммарная теплопродукция в организме происходит тремя способами. Сразу же оговоримся, существует еще и четвертый – основной обмен, но в данной монографии вопросов, связанных с ним, мы практически касаться не будем. Единственное, отметим: основной обмен – величина постоянная и не может быть изменена. Итак, три способа теплопродукции:
1. "Сократительный (дрожательный) термогенез" (холодовая мышечная дрожь) – с помощью усиления непроизвольной мышечной активности (сокращения с частотой 10–20 раз в секунду скелетных мышц). У новорожденных этот механизм развит плохо, хотя у взрослых именно он является наиболее значимым для дополнительного теплообразования. Сокращение мышц способно за несколько минут повысить величину теплопродукции в 4–5 раз, поскольку никакой полезной работы при "мышечной дрожи" не совершается, то вся энергия, получаемая в результате "данной работы" остается в организме в виде тепла. Эта реакция используется организмом только тогда, когда нужно очень быстро повысить температуру тела. Хотя "сократительный" термогенез уже очень давно признан важным механизмом повышения температуры тела, и его значимость доказана в большом количестве экспериментальных и клинических исследований, конкретные центральные механизмы генерации "дрожания" практически неизвестны (Palmes Е. D., Park С. R., 1962; Saper С. В., Breder С. D., 1994; Morrison S. F., Nakamura K., 2011). Новорожденные дети включают механизм дрожательного термогенеза только при предельных температурах охлаждения. Связывают (Аршавский И. А., 1969) это с тем, что у них имеется существенно более высокий уровень постоянной тонической мышечной активности (гипертонус), выполняющий терморегуляционную функцию, повышая порог дрожательного рефлекса.
2. "Несократительный термогенез" – теплообразование, не связанное с мышечной активностью, то есть продуцирование тепла в результате увеличения скорости обмена веществ и, следовательно, увеличение потребления кислорода организмом. Основным источником образования такого тепла у новорожденных детей является бурый жир. Это очень интересная ткань, изучение которой в настоящее время интенсивно продолжается. Но об этом ниже.

Рис. 5. Конрад Гесснер (1516–1565)
Бурая жировая ткань открыта в 1551 году великим швейцарским ученым Конрадом Гесснером (рис. 5). Несколько слов о К. Гесснере. Он был ученым-энциклопедистом, одним из первых попытавшимся систематизировать накопленные к тому времени сведения о животных и растениях. Научные интересы К. Геснера были чрезвычайно широки и касались филологии, фармакологии, медицины, минералогии, зоологии, ботаники, библиографии. Ему принадлежит одна из первых попыток классификации растений (Enchiridion historiae plantarum, 1541). Он разделил растительное царство, основываясь на признаках цветка и семени; отделил класс, порядок, род и вид, наметив тем самым принципы бинарной номенклатуры. Кроме того, К. Гесснер является одним из основоположников ботанической иллюстрации, сделав сотни рисунков растений и животных. Ученый впервые описал все 130 языков, существовавших в Европе его времени, а своей книгой "Всеобщая библиотека" (1545–1555) заложил основы библиографии (Cannon В., Nedergaard J., 2008).
К. Гесснер описал бурую жировую ткань в межлопаточной области, как "ни жир, ни плоть (мышцы)". Интересно, что через 460 лет, анализируя работу К. Гесснера, В. Cannon и J. Nedergaard (2008) отмечают, что он был абсолютно прав и по своим функциям "бурые и белые адипоциты действительно различны. Клетки бурого жира на самом деле более "телесны", чем это предполагалось ранее". Необходимо отметить, что происхождение белых жировых клеток и бурых разное. Если первые происходят из боковой мезодермы, то вторые – миобластного происхождения – из параксиальной мезодермы (Atit R. et al., 2006). Некоторые исследователи (Barbatelli G. et al., 2010) в экспериментальных работах показали, что белый адипоцит может трансформироваться в бурый. Они могут появляться в белой жировой ткани в ответ на холод или стимуляцию катехоламинами (Young P. et al., 1984; Cousin В. et al., 1992).
До начала XIX века бурую жировую ткань расценивали как часть тимуса. Позже, к концу XIX века, ее стали считать измененной формой жировой ткани с эндокринными свойствами. И только в середине XX века стало понятно, что это "центральная" ткань, обеспечивающая "несократительный термогенез".
У зародыша человека бурая жировая ткань появляется на пятом месяце гестации (Merklin R. J., 1974). Бурый жир составляет от 2 до 6 % массы тела новорожденных, расположен подкожно, между лопатками, в виде небольших отложений вокруг мышц и кровеносных сосудов шеи, щеках (комочки Биша), а также в большом количестве в подмышечных впадинах. Более глубокие отложения – в переднем средостении, вдоль позвоночника, вокруг почек, надпочечников, аорты. По сравнению с белой жировой тканью, васкуляризация бурой в 4–6 раз больше. Она очень хорошо иннервирована. На бурых адипоцитах находится большое количество норадреналиновых рецепторов, а также симпатические норадренергические нервные окончания. Несколько адипоцитов со смежными капиллярами и нервом составляют долю, окруженную толстыми соединительнотканными структурами.
Молекула, ответственная за термогенез, называется несцепленным белком 1 (UCP-1), расположенным во внутренней мембране митохондрий. Ранее его называли "термогенин". Его количество составляет примерно 5 % от общего количества белка, находящегося в митохондриях бурого адипоцита (Stuart J. A. et al., 2001). Точный механизм активации UCP-1 жирными кислотами не известен. Считают (Cannon В., Nedergaard J., 2004), что жирные кислоты могут функционировать как кофакторы или аллостерические регуляторы. Термогенез бурой жировой ткани увеличивается через индукцию UCP-1 катехоламинами или гормонами щитовидной железы (Cannon В., Nedergaard J., 2010). Зная это, становится понятным еще один механизм, делающий недоношенных, особенно детей с ЭНМТ, склонными к развитию гипотермии. Ниже мы еще раз вернемся к рассмотрению этого механизма развития гипотермии у глубоконедоношенных детей. Апоптоз бурых адипоцитов увеличивает ФНОа (Hotamisligil G. S., 1999). Забегая чуть-чуть вперед, эти сведения нам пригодятся чуть позже, отметим, что при ожирении содержание ФНОа в жировой ткани повышено (Hotamisligil G. S., 1999).
Окисление жирных кислот в бурой жировой ткани осуществляется без значимого синтеза макроэргов и, таким образом, с максимально возможным образованием теплоты (рис. 6). Посредством механизмов несократительного термогенеза, уровень теплопродукции у человека может быть увеличен примерно в 3 раза по сравнению с уровнем основного обмена (50 г бурого жира могут обеспечить 20 % обмена) (Cypess А. М. et al., 2009). Но у детей, особенно недоношенных, запасы бурого жира невелики, поэтому увеличить теплопродукцию несократительным термогенезом с участием бурой жировой ткани они не могут (Nedergaard J. et al., 2007; Cypess A. M. et al., 2009).
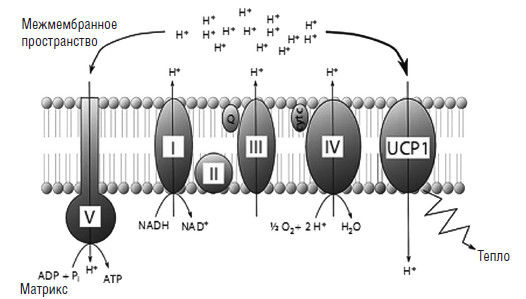
Рис. 6. Схематическое изображение дыхательной цепи митохондрий (Tews D., Wabitsch М., 2011) В митохондриях активированных бурых адипоцитов, протонный градиент установлен дыхательной цепью несцепленного белка 1 (UCP-1). Это приводит к продукции тепловой энергии вместо производства АТФ. I – NADH дегидрогеназа, II – циксинат дегидрогеназа, III – комплекс цитохрома bc1, IV – цитохром с оксидаза, V – АТФ-синтаза, Q – убихинон, cyt с – цитохром С